?vino rūg?ties akumuliatori? chemijos atidengimas
Ar kada nors sustojote apm?styti sud?tingus procesus, vykstan?ius tvirtose ?vino rūg?ties akumuliatori? ribose? ?iuose nepretenzinguose korpusuose slypi triuk?mingas cheminis ?okis, orkestruojantis energij?, kuria pasitikime. Pasigilinkime ? m?sl?, supan?i? slapt? gyvyb? ?vino rūg?ties akumuliatori? viduje, atlikdami glaust? tyrim?.
Kaip ?vino plok?t?s generuoja elektr? sieros rūg?tyje:
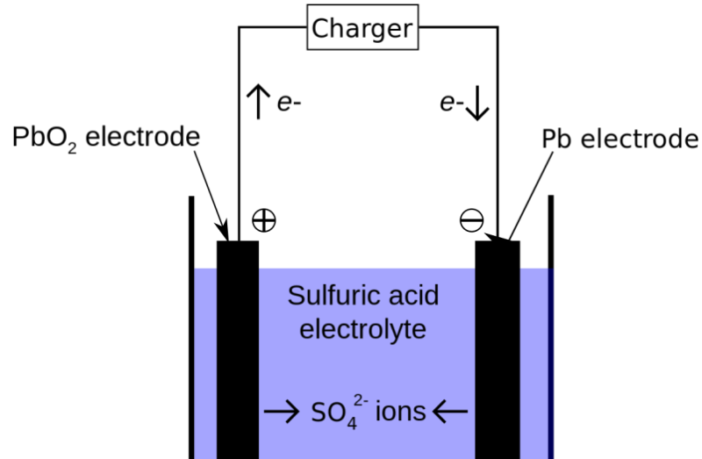
Giliai ?vino rūg?ties baterij? viduje yra daugyb? element?, kuri? kiekvienoje yra plok??i? pora – teigiami ir neigiami elektrodai, o j? daliklis yra praskiesta sieros rūg?tis. Visi?kai ?krautas kiekvienas elementas tiekia ma?daug 2,1 volto. 6 volt? akumuliatoriui reikia trij? element?, o 12 volt? – ?e?i?.
Kiekvienoje l?stel?je esan?ios ?vino plok?t?s yra sud?tingai sukurtos tinkleliai, kuri? chemin? sud?tis ?iek tiek skiriasi, padengti skirtingomis aktyviomis med?iagomis. Naudojant akumuliatori?, jis i?sikrauna, i?leid?iama sukaupta energija ir sunaudojama dalis sieros rūg?ties. Palaipsniui rūg?ties sulfatas padengia plok?teles, suma?indamas turim? pavir?i?, kad chemin? reakcija t?st?si. Visi?kai padengus, reakcija sustoja, tod?l akumuliatorius tampa bej?gis.
Nepaisant to, kad pasiek?me ?? ta?k?, yra vilties, kad ?vino rūg?ties akumuliatoriai atgims ?kraunant. ?krovus, sulfatas gr??ta ? rūg?t?, tod?l procesas gali prasid?ti i? naujo. Ta?iau ne visas sulfatas yra visi?kai regeneruojamas per kiekvien? cikl?, tod?l dalis lieka ant plok?teli?.
I? esm?s, nors ?vino rūg?ties baterijos yra būtinas energijos kaupimas, j? tarnavimo laikas yra ribotas. Ta?iau supratus sud?ting? ?i? baterij? chemij?, paai?k?ja j? veikimas ir galimyb? prat?sti j? ilgaam?i?kum? rūpestingai pri?iūrint ir ?kraunant. Tokia yra ?avinga kelion? ?vino rūg?ties baterij? ?irdyje – chemini? med?iag? ?okis, formuojantis mūs? energijos poreikius.

