Az ólom-savas akkumulátorok kémiájának bemutatása
Megállt már valaha, hogy elgondolkozzon az ólom-savas akkumulátorok robusztus keretein belül kibontakozó bonyolult folyamatokon? Ezekben az igénytelen burkolatokban nyüzsg? kémiai tánc zajlik, hangszerelve azt az energiát, amelyre támaszkodunk. Egy t?m?r feltáráson keresztül ássuk be az ólom-savas akkumulátorok titkos életének rejtélyét.
Hogyan termelnek elektromosságot az ólomlemezek kénsavban:
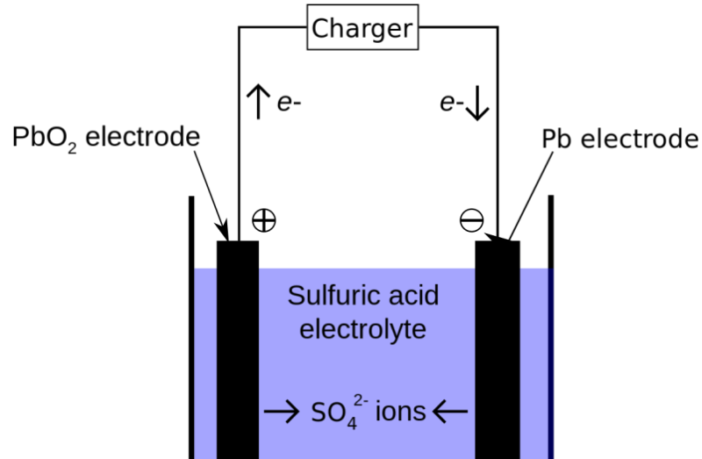
Az ólom-savas akkumulátorok mélyén cellák sora található, mindegyikben egy pár lemez található – pozitív és negatív elektródák, amelyek elválasztójaként hígított kénsav szolgál. Teljesen felt?lt?tt állapotban mindegyik cella k?rülbelül 2,1 voltot szolgáltat. Egy 6 voltos akkumulátorhoz három cella szükséges, egy 12 voltos akkumulátorhoz pedig hat cella elegend?.
Az egyes cellákon belüli ólomlemezek bonyolultan kialakított rácsok, marginálisan eltér? kémiai ?sszetétellel, és kül?nb?z? aktív anyagokkal vannak bevonva. Amikor az akkumulátort használják, lemerül, felszabadítja a tárolt energiát és kénsavat fogyaszt. A savból származó szulfát fokozatosan beborítja a lemezeket, cs?kkentve a kémiai reakció fennmaradásához rendelkezésre álló felületet. A teljes bevonat után a reakció leáll, és az akkumulátor er?tlenné válik.
Annak ellenére, hogy elértük ezt a pontot, van remény az ólom-savas akkumulátorok feltámasztására az újrat?ltés révén. újrat?ltéskor a szulfát visszatér savvá, lehet?vé téve a folyamat újraindítását. Azonban nem minden szulfát nyerhet? vissza teljesen minden ciklusban, így egy rész a lemezeken marad.
Lényegében, míg az ólom-savas akkumulátorok nélkül?zhetetlen energiatárolót kínálnak, élettartamuk véges. Az akkumulátorok bonyolult kémiájának megértése azonban rávilágít m?k?désükre és arra, hogy gondos karbantartással és újrat?ltéssel meghosszabbíthatják élettartamukat. Ilyen a leny?g?z? utazás az ólom-savas akkumulátorok szívében – az energiaszükségletünket alakító vegyszerek tánca.

